药明康德医疗器械测试中心的微生物实验室拥有CNAS、CMA、OECD GLP、FDA GLP及A2LA资质,可为药品、医疗器械客户提供全方位微生物测试  中国:《消毒技术规范》2002年版、2010 GMP指南、GB/T 38502-2020 等消毒标准
中国:《消毒技术规范》2002年版、2010 GMP指南、GB/T 38502-2020 等消毒标准 美国:USP<1072>、ASTM E1153、ASTM E2614、PDA TR70
美国:USP<1072>、ASTM E1153、ASTM E2614、PDA TR70 欧洲:EN1276、EN1650、EN13697等消毒标准
欧洲:EN1276、EN1650、EN13697等消毒标准
消毒剂效力测试
我们可以为企业定制符合中、美、欧 GMP及符合USP和EN标准的消毒剂效力验证



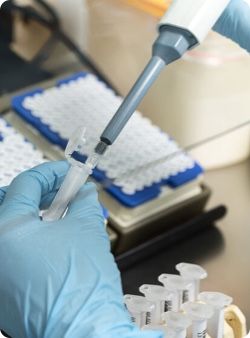



菌种鉴定
我们拥有自动化基因鉴定系统,满足21 CFR 11 的经验证的软件和数据库,几小时内完成细菌/真菌基因测序及鉴定。药/械生产企业在以下情况下需鉴定微生物:
 洁净室环境分离株
洁净室环境分离株 无菌检查试验结果阳性
无菌检查试验结果阳性 非无菌药品的控制菌检查中发现疑似菌落
非无菌药品的控制菌检查中发现疑似菌落 微生物OOS调查等
微生物OOS调查等无菌试验
无菌检验是产品经过灭菌处理后,按药典上的规定对产品进行技术操作;无菌检验是为确定单元产品或其部分上是否存在活微生物而进行的技术操作,是开发、确认或再鉴定的一部分。
 无菌检查:依据GB/T 19973.2-2018、 ISO 11737-2:2019
无菌检查:依据GB/T 19973.2-2018、 ISO 11737-2:2019 无菌检验:依据中国药典 通则<1101>、USP <71>、EP 2.6.1、GB/T 14233.2-2005
Sterility test
无菌检验:依据中国药典 通则<1101>、USP <71>、EP 2.6.1、GB/T 14233.2-2005
Sterility test生物负载 & 微生物限度
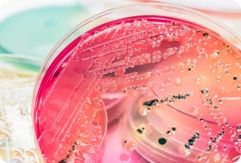
生物负载是一件产品和/或包装上或其中存活的微生物总数。微生物计数法系用于能在有氧条件下生长的嗜温细菌和真菌的计数。控制菌检查法系用于在规定的试验条件下,检查供试品中是否存在特定的微生物。
生物负载检测
 生物负载:GB/T 19973.1-2015、ISO 11737-1:2018
生物负载:GB/T 19973.1-2015、ISO 11737-1:2018 微生物限度:中国药典 通则 <1105> & <1106>,USP <61> & <62>,EP 2.6.12 & 2.6.13
微生物限度:中国药典 通则 <1105> & <1106>,USP <61> & <62>,EP 2.6.12 & 2.6.13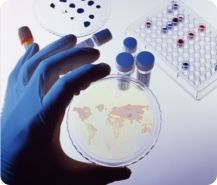
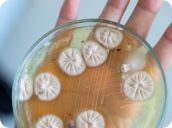



环境监测
我们可按中国GMP、GB/T 16292、GB/T 16293、GB/T 16294、GB 50591及ISO 14644等标准,为企业定制环境监测方案,提供快捷全面的监测服务:
 沉降菌/浮游菌/表面微生物
沉降菌/浮游菌/表面微生物 悬浮粒子
悬浮粒子 噪声/照度
噪声/照度 风速/换气次数/压差
风速/换气次数/压差 温度/湿度
温度/湿度

复用器械再处理确认
再处理的定义为用于已使用或受到污染但适用于后续单次使用的医疗器械的经确认的处理过程。这些过程通常包括清洁、消毒或灭菌。清洁用来去除污物,消毒或灭菌用以灭活微生物。我们可以依据FDA 指南、国内指导原则、AAMI TIR 12、AAMI TIR30、ISO 17664、ISO 15883、YY/T 0802、ASTM、WS标准等提供以下确认服务
 清洁确认
清洁确认 消毒确认
消毒确认 灭菌确认
灭菌确认 干燥时间确认
干燥时间确认 耐用性确认
耐用性确认细菌内毒素测试
内毒素检测是通过量化由革兰阴性菌产生的细菌内毒素等方式,以判断供试品中细菌内毒素的限量是否符合规定的一种方法。细菌内毒素检查包括两种方法,即凝胶法和光度测定法 ,后者包括浊度法和显色基质法。
基于中国药典 通则 <1143>,USP <85>,USP <161>、EP 2.6.14、GB/T 14233.2-2005,ANSI/AAMI ST72
支原体检测

环境监测
1.原体又称霉形体,直径0.1-0.3μm,是目前发现的最小的、最简单的原核生物
2.可以轻松地通过滤膜,混入培养系统中,呈高度多形性,有球形、杆形、丝状、分支状等多种形态
3. 通常依附在细胞膜表面,支原体没有刚性的细胞壁,因此普通的抗生素对它不起作用

支原体污染
1.在生物制药行业,支原体污染产生的影响几乎具有毁灭性,如整批产物必需丢弃,生产车间停产整顿等
2. 污染很难察觉,即使生长密度高达 107-109 CFU/mL,也很难有污染迹象(浑浊、pH 变化等),是生物制品和无菌灌装培养基

支原体检测
1.培养法(Agar and Broth Procedure)是经典的支原体检测方法,是中、美、欧药典上公认的官方方法,检测灵敏度和可靠性已获得了证实,检测限可达0.1cfu/ml
2. 药明康德医疗器械测试中心微生物实验室拥有FDA GLP、OECD GLP、CNAS、CMA资质,可根据客户需求进行支原体检测,满足中、美欧多地的要求